
Czy warto analizować zużycia antybiotyków?
Racjonalna antybiotykoterapia wymaga analiz, dzięki którym można monitorować stosowanie leków przeciwinfekcyjnych używanych w szpitalu, przestrzeganie procedur i realizację postawionych celów. Jedną z popularniejszych metod jest analiza retrospektywna ilościowa oparta o Dobowe Dawki Dzienne (DDD). Artykuł przytacza najważniejsze zagadnienia związane z tym jak wykonać taką analizę, a także w jakim celu jest wykonywana.
Słowa kluczowe
Wstęp
Cytując European Centre for Disease Prevention and Control antybiotyki są jednym najważniejszych okryć terapeutycznych w historii medycyny. Zrewolucjonizowały sposoby leczenia infekcji, znacznie zmniejszając śmiertelność. Można ulec złudnemu przeczuciu, że stosowanie antybiotyków ma tylko dobre strony. Niestety ich nadużywanie prowadzi do poważnych komplikacji-głównie rozwoju antybiotykooporności, występowania działań niepożądanych i niepotrzebnych kosztów [1].
Antybiotyki to jedyna grupa leków, której skuteczność maleje z czasem – w związku z narastającą opornością bakterii. Zasadniczo jest to nieuniknione, jednak niewłaściwe stosowania przyspiesza ten proces. Jeżeli weźmiemy pod uwagę fakty iż:
- około połowa zleceń na antybiotyki może być niewłaściwa, nawet 10% hospitalizowanych pacjentów, którzy otrzymują antybiotyki nie ma wskazań do ich stosowania
- w szpitalach o profilu ogólnym zakażenia stwierdza się u 15-20% pacjentów (10-15% pozaszpitalnych, 5% szpitalnych)
- wydatki na antybiotyki to często 20-30% ze wszystkich leków stosowanych w szpitalu
- wydaje się oczywiste, że trzeba podjąć działania mające na celu ograniczenie błędnego stosowania antybiotyków [2].
Monitorowanie leków przeciwinfekcyjnych
Jednak, żeby dojść do wniosków, działań i (co najważniejsze) efektów, najpierw trzeba uzyskać dane na temat stosowania antybiotyków w danym ośrodku. Celem monitorowania stosowania leków przeciwinfekcyjnych opracowanie lub weryfikacja wewnętrznych wytycznych stosowania antybiotyków lub szkoleń dla personelu szpitala, lub ocena efektów wdrożonych działań. Proponowane są różne analizy:
- Monitorowanie prospektywne
- ciągłe – zwyczaj na oddziałach o bardzo wysokim zużyciu antybiotyków, lub konkretnych praktyk istotnych dla racjonalnej antybiotkoterapii, np.:
- monitorowanie decyzji o modyfikacji lub kontynuacji terapii w 3 dobie leczenia (szczególnie na OIT),
- przegląd wszystkich stosowanych antybiotyków 2‑3 razy w tygodniu (tzw. obchody antybiotykowe) – szczególnie na oddziale OIT,
- zmiana nieskutecznej antybiotykoterapii, lub dołączenie kolejnego antybiotyku
- stosowanie wybranych antybiotyków (szczególnie grupy reserved wg WHO),
- wybranych grupy zakażeń (np.: bakteriemia MSSA) lub pacjentów (np.: z niewydolnością nerek);
b. punktowe – badania w ciągu jednego dnia wszystkich antybiotykoterapii (najczęściej na na 1 oddziale) pod kątem:
- zasadności / określenia wskazań do stosowania antybiotyku,
- zgodności leczenia z obowiązującymi standardami,
- właściwej diagnostyki laboratoryjnej,
- modyfikacji leczenia po otrzymaniu wyników badań mikrobiologicznych,
- właściwe dawkowanie.
Ma to na celu:
- identyfikację nadużywania antybiotyków,
- ocenę czasu terapii (szczególnie przy profilaktyce okołozabiegowej),
- kontrolę stosowania terapii sekwencyjnej,
- ocenę kojarzenia antybiotyków.
2. Monitorowanie retrospektywne
a. jakościowe – wybranych grupy zakażeń (np.: bakteriemia MSSA) lub pacjentów (np.: z niewydolnością nerek), lub badanie czasu od rozpoznania zakażenia do podania antybiotyku i inne;
b. ilościowe – analiza zużycia antybiotyków. Taki raport jest najprostszy do przygotowania, jednak nie pozawala na ocenę jakości leczenia zakażeń. Raport taki pozwala jednak na obserwację trendów w szpitalu, i jest cenny do łącznych wniosków razem z innymi typami monitorowania (np.: wraz z mapowaniem mikrobiologicznym) [3].
Monitorowanie retrospektywne ilościowe
Monitorowanie retrospektywne ilościowe prowadzone jest najczęściej przy użyciu definiowanych dawek dziennych (DDD). DDD jest wartością umowną, która nie musi się pokrywać z tym ile antybiotyku pacjent dostaje dziennie, nie należy jej również traktować jako sugestii odnośnie dawkowania leku. Jedynym celem DDD jest umożliwienie porównania zużycia jednego leku z innym. Wartość DDD dla danego leku ustala Norwegian Institute of Public Health w ramach WHO Collaborating Centre for Drug Statistics Methodology. Na stronie https://atcddd.fhi.no/atc_ddd_index/ dostępna jest wyszukiwarka leków (także kombinacji w lekach złożonych), a także opis metodologii ATC i DDD z które odpowiada Instytut. W wielu przypadkach ta wartość odbiega od rzeczywistej dawki dobowej stosowanej w danym ośrodku. Może to mieć miejsce w szpitalach pediatrycznych (wtedy DDD jest wyższe niż dawki rzeczywiście stosowane), albo w przypadkach wielu leków, np.: tam gdzie ampicylina z sulbaktamem (DDD=6 w przeliczeniu na ampicylinę czyli 6g ampicyliny na dobę) jest stosowana w celu terapii zakażeń o etiologii Acinetobacter baumannii (wtedy dobowa dawka to często 12 albo 18g ampicyliny na dobę). Wtedy można zastosować PDD czyli prescribed daily dose. Zastosowanie DDD pozwala jednak na porównanie zużycia antybiotyków w różnych ośrodkach o podobnym profilu pacjentów. Ważne jest to że ten sam lek ma inne DDD w zależności od drogi podania.

Przykład 1.
W szpitalu w ciągu roku zużyto 900 fiolek ampicyliny z sulbaktamem o mocy 2+1g. Jak wspomniano DDD tego leku to 6, w przeliczeniu na ampicylinę. Zatem 1 fiolka (2g ampicyliny) to 1/3 DDD, a 900 fiolek to 300 DDD
Ważne jest że większość programów aptecznych (np. AMMS) daje możliwość generowania raportu zużycia leków w DDD i nie trzeba tego robić ręcznie. Jednak trzeba mieć uzupełnione wartości „DDD” i „ilość DDD w opakowaniu” w karcie leku. Wartości DDD mogą się zmieniać i należy sprawdzić czy na stronie instytutu nie ma informacji o zmianie DDD – na szczęście jest dostępna jest lista aktualizacji na stronie: https://atcddd.fhi.no/atc_ddd_alterations__cumulative/ddd_alterations/.
Warto zadbać by wszystkie odpowiedniki miały taką samą nazwę międzynarodową, żeby program dobrze to połączył (jeśli jedna będzie miała nazwę po łacinie, druga po angielsku a trzecia drukowanymi literami to wszystkie na raporcie będą osobno). Jeżeli generujemy raport osobno dla postaci doustnych i parenteralnych też warto ujednolicić „postać” w karcie leków. Można też się zdecydować na raport wg grup ATC (klasyfikacja anatomiczno-terapeutyczno-chemiczna), wtedy na raporcie nie będzie konkretnej substancji czynnej, tylko zużycie poszczególnych podgrup antybiotyków (tetracykliny). Warto jeszcze osobno przygtować raport wg grup dostępności (wg WHO AWaRe – Access, Watch, Reserve) [4].
W ten sposób można uzyskać raport zużycia w DDD w jednostce czasu (zazwyczaj 1 rok kalendarzowy). Dalej jednak trudno taki raport użyć do jakiegokolwiek celu. Większe zużycie leków może wynikać z większej liczby pacjentów. W tym celu trzeba podać dane w DDD na 100 lub 1000 osobodni. Taki raport może jednak służyć tylko porównaniu do innych szpitali o podobnym profilu pacjentów. Żeby móc obserwować trendy konieczne jest porównanie do wcześniejszych lat.
Przykład 2.
Zużycie kloksacyliny IV na przestrzeni lat, jako potwierdzenie poprawy leczenia bakteriemii MSSA i zawężania spektrum antybiotykoterapii.
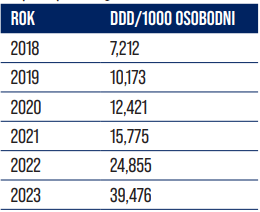
Jeżeli założonym celem była redukcja zużycia danej grupy leków – taki raport pozwala pokazać jak wygląda realizacja celu.
Przykład 3.
Zużycie ciprofloksacyny IV na przestrzeni lat, jako potwierdzenie realizacji celu-redukcji zużycia leku.
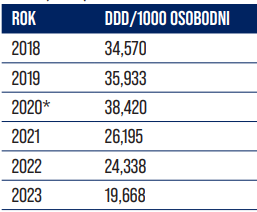
*rok odniesienia, w którym ustalono cel
Jak widać na załączonych przykładach – monitorowanie retrospektywne ilościowe nie ma być celem samym w sobie ale ma być robione w celu weryfikacji celów, obserwowania trendów, lub łącznych wniosków. Przykład:
- Monitorowanie mikrobiologiczne wykazuje wzrost izolacji bakterii o nabytej oporności na karbapenemy na oddziale OIT. Raport DDD/1000 rok do roku wykazuje wzrost zużycia karbapenemów na danym oddziale. Należy zatem podjąć konkretne działania, przykłady:
- przeprowadzić szkolenie na oddziale by pokazać konkretny skutek wzrostu zużycia karbapenemów
- poszerzyć analizę by wykazać przyczyny danego stanu, przykłady: czy na oddziale jest opracowana propozycja terapii empirycznej najczęściej występujących zakażeń?
- czy na oddziale jest opracowana procedura przejścia na terapię celowaną po uzyskaniu wyniku badań mikrobiologicznych?
- czy obecne opracowania lub procedury są przestrzegane?
- czy należy podjąć dodatkowe działania w celu naprawy sytuacji?
Zatem monitorowanie retrospektywne ilościowe jest często początkiem dalszych analiz i działań, a także relatywnie łatwą i obiektywną metodą weryfikacji wykonania ustalonych celów.
Taki raport ma jednak pewne „pułapki”:
- Jeżeli w danym ośrodku używano subterapeutycznych dawek antybiotyków np. amioglikozydowych, to w wyniku wprowadzonych działań DDD/1000 osobodni tej grupy leków wzrośnie, i nie powinno to być osądzone negatywnie;
- Stosowanie wyższych dawek i stosowanie terapii sekwencyjnej (przejście na celowaną terapią antybiotykami w formie doustnej) może poprawić skuteczność leczenia i skrócić czas hospitalizacji. Wtedy ta sama liczba pacjentów „zużyje” więcej DDD/1000 osobodni i zwolni miejsce w szpitalu dla następnych pacjentów, którzy też będą konsumować antybiotyki. Zatem ogólna wartość DDD/1000 osobodni może wzrosnąć, mimo ogólnej poprawy jakości leczenia;
- Jeżeli w ramach stosowania racjonalnej antybiotykoterapii wydłuży się czas terapii, wtedy kiedy jest on wymagany, mimo poprawy stanu pacjenta (minimalny czas antybiotykoterapii bakteriemii gronkowca złocistego, albo Infekcji Clostridioides difficile). Zużycie DDD/1000 osobodni antybiotyków stosowanych w leczeniu tych infekcji wzrośnie;
- Łączne zużycie antybiotyków w danej jednostce warto analizować w kontekście:
- sytuacji mikrobiologicznej (jeśli wzrośnie ilość infekcji o etiologii Enterobacterales z nabytą opornością typu ESBL, wzrośnie zużycie karbapenemów)
- innych współczynników jakościowych, takich jak: współczynnik umieralności, średnia długość hospitalizacji itp.
- Postawionych celów;
- Raport musi mieć czytelnie opisane wnioski i komentarze.
Warto zauważyć że monitorowanie retrospektywne ilościowe nie musi się odnosić tylko do danego szpitalna ale i do kraju. Zgodnie z Zaleceniami Rady Unii Europejskiej w sprawie intensyfikacji działań w zakresie zwalczania oporności na środki przeciwdrobnoustrojowe w ramach podejścia „Jedno zdrowie” (2023/C220/01), Rada UE rekomenduje wprowadzenie odpowiednich działań mających na celu zapewnienie, aby do 2030 r. całkowita konsumpcja antybiotyków u ludzi (w zdefiniowanej dawce dziennej, DDD na 1000 mieszkańców na dzień), w lecznictwie otwartym i zamkniętym łącznie, została w Unii Europejskiej zmniejszona o 20 % w względem 2019 roku. Kolejnym celem jest osiągnięcie udziału co najmniej 65 % antybiotykiów należące do grupy „Access” wg podziału WHO [5]. Opierając się na raporcie Narodowego Programu Zdrowia – oba cele mamy na ten moment niespełnione – zużycie pozostaje na poziomie z roku 2019 (23,6 DDD/1000 mieszkańców na dzień), a udział zużycia grupy „Access” to 60,4% [6].
mgr Piotr Łój1,2,3,4
1Konsultant Farmacji Klinicznej i Antybiotykoterapii
2Wojewódzki Szpital Specjalistyczny nr 5 im. Św. Barbary w Sosnowcu – Centrum Urazowe
3Instytut Fizjoterapii i Nauk o Zdrowiu AWF Katowice
4Koordynator Sekcji ds. Terapii Zakażeń Polskiego Towarzystwa Farmaceutów Klinicznych
PIŚMIENNICTWO
-
https://www.ecdc.europa.eu/en/antimicrobial-resistance/facts (stan z dn. 27.08.2024 r.)
-
Hryniewicz W., Ozorowski T. Szpitalna polityka antybiotykowa. Propozycja kierowana do szpitali Narodowy Instyut Leków, War‑ szawa 2011
-
Ozorowski T., Woroń J., Misiewska‑Kaczur A. Polityka antybiotykowa. Program szpitalnej polityki antybiotykowej. Centrum Monitorowania Jakości w Ochronie Zdrowia. Kraków 2015
-
Web Annex. Infographics. In: The WHO AWaRe (Access, Watch, Reserve) antibiotic book. Geneva: World Health Organization; 2022 (WHO/MHP/HPS/EML/2022.02) stan z dn. (27.08.2024 r.)
-
Zalecenia Rady w sprawie intensyfikacji działań w zakresie zwalczania oporności na środki przeciwdrobnoustrojowe w ramach podejścia „Jedno zdrowie” (2023/C 220/01) https://eurlex.europa.eu/legal-content/PL/ TXT/PDF/?uri=CELEX:32023H0622(01) (stan z dn. 27.08.2024 r.)
-
Pawlik K., Bysiek J., Hryniewicz W., Skoczyńska A. Raport Monitorowanie zużycia antybiotyków w lecznictwie zamkniętym za rok 2022. Warszawa, dn. 28.12.2023 r
Powyższy artykuł został opublikowany na łamach 62. wydania kwartalnika „Farmakoekonomiki Szpitalnej". Czasopismo, skierowane do pracowników farmacji szpitalnej, można otrzymać w formie bezpłatnej prenumeraty.